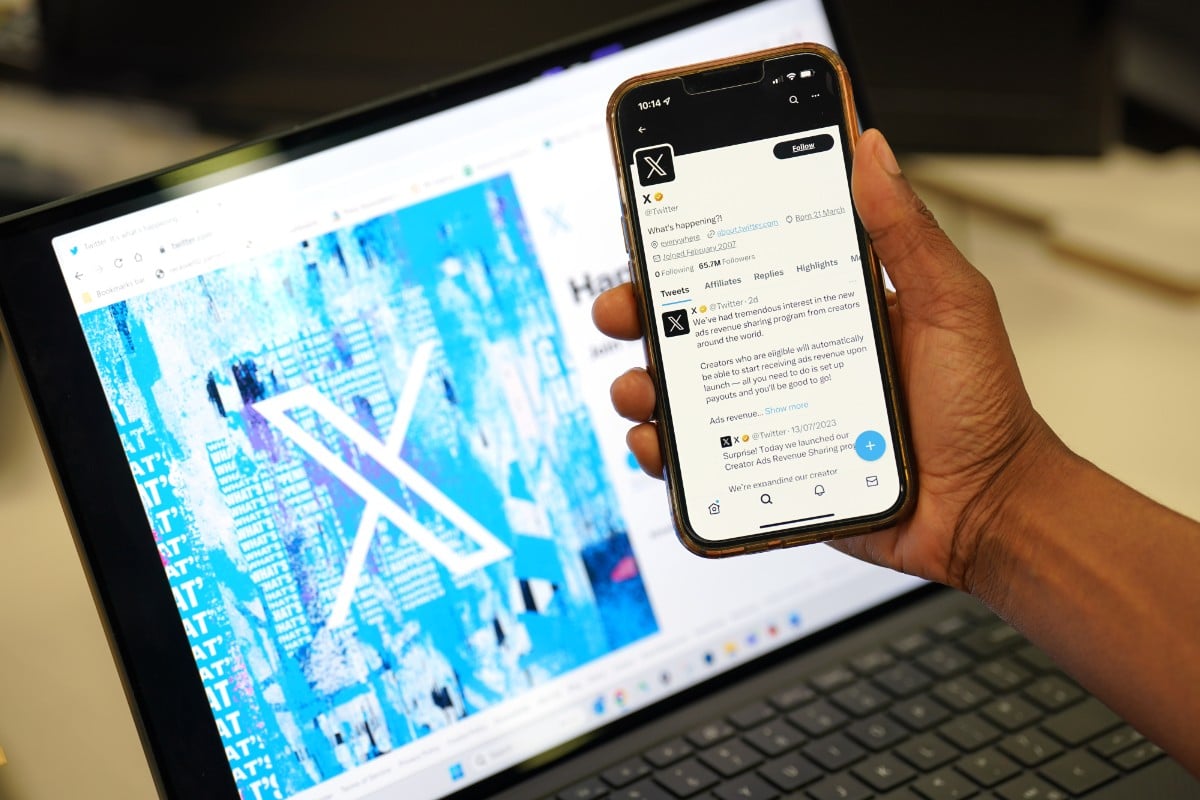
A continuación se detallan los tipos de cookies utilizados en nuestra web. Puede configurar la aceptación o no de las mismas. Lea nuestra Política de cookies.








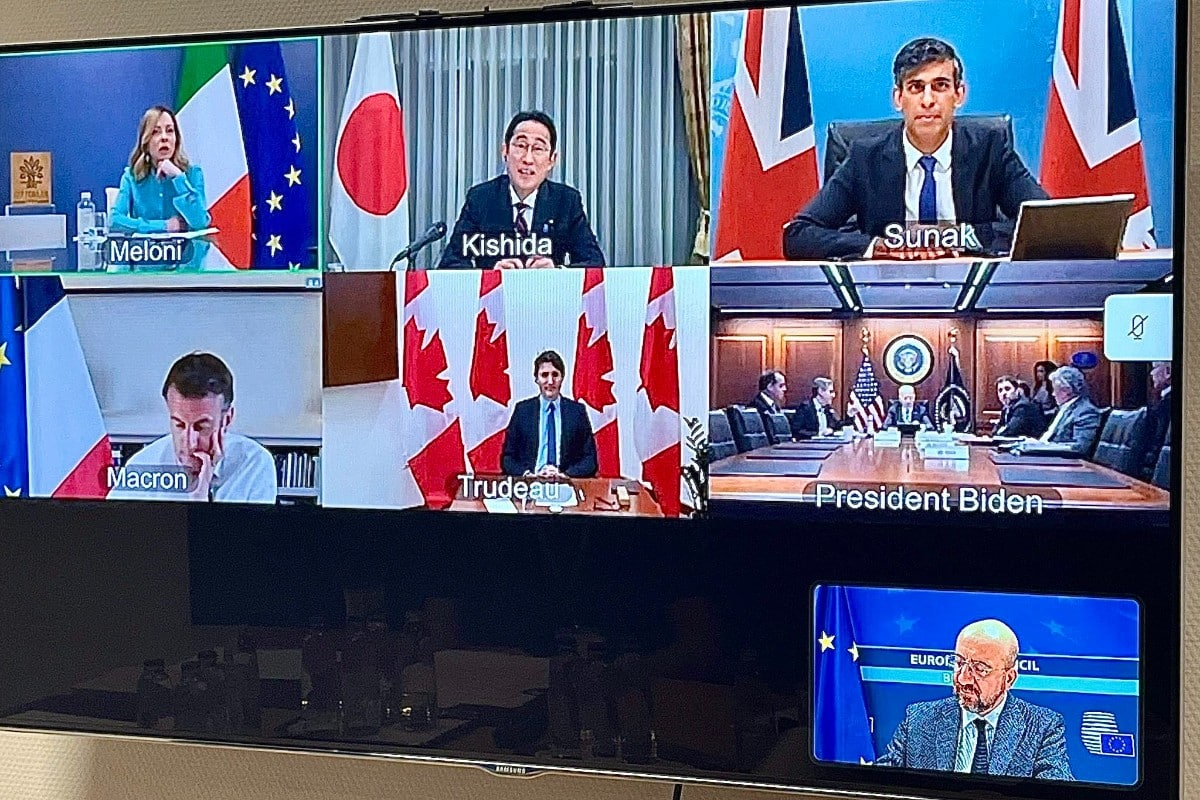



A continuación se detallan los tipos de cookies utilizados en nuestra web. Puede configurar la aceptación o no de las mismas. Lea nuestra Política de cookies.
Las cookies estrictamente necesarias tiene que activarse siempre para que podamos guardar tus preferencias de ajustes de cookies.
Si desactivas esta cookie no podremos guardar tus preferencias. Esto significa que cada vez que visites esta web tendrás que activar o desactivar las cookies de nuevo.
Identidad: Google
Cookies de Google Analytics: para obtener información que permite medir cómo interactúan los usuarios con el contenido del Servicio + info
Identidad: OneSignal
Cookies de OneSignal, para enviar al usuario avisos o contenidos personalizados por medio de notificaciones push + info
¡Por favor, activa primero las cookies estrictamente necesarias para que podamos guardar tus preferencias!